به گزارش سایت خبری پرسون، پژوهشگران «دانشگاه کلمبیا» با مهندسی کردن باکتری روده توانستند آن را برای جستجو و از بین بردن تومورهای سرطانی موشها به کار بگیرند.
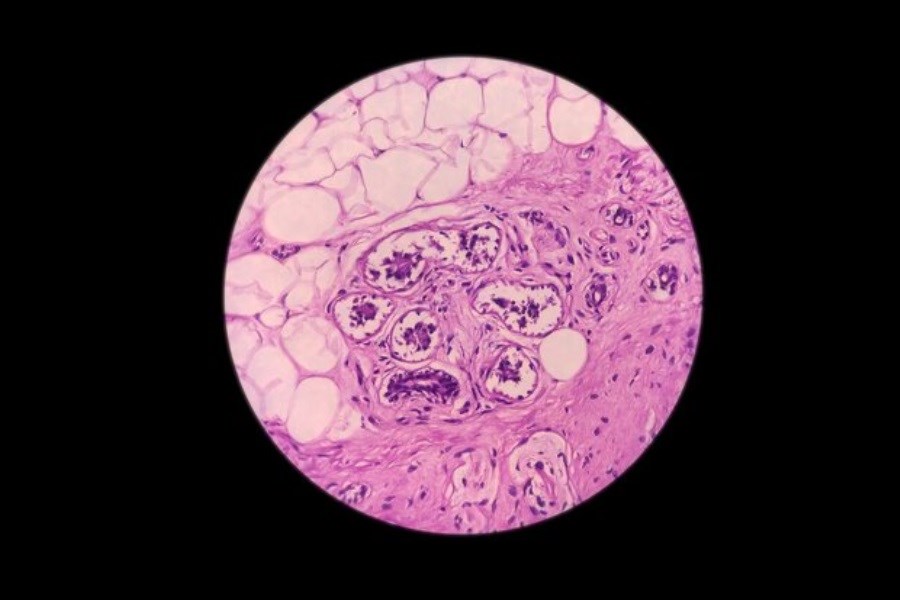
به گزارش ایسنا و به نقل از نیو اطلس، تومورهای سرطانی در فرار کردن از واکنش ایمنی بدن مهارت دارند و درمان را دشوار میکنند. پژوهش جدیدی که در «دانشگاه کلمبیا»(Columbia University) انجام شده است، نشان میدهد که میتوان یک باکتری معمولی روده را مهندسی ژنتیکی کرد تا بتواند تومورهای سرطانی را پیدا کند و از بین ببرد.
روشهای بسیاری وجود دارند که تومورها به وسیله آنها میتوانند از واکنشهای ایمنی بدن فرار کنند و زنده بمانند. یکی از این روشها، جلوگیری از درگیر شدن سلولهای ایمنی در فرآیند «کموتاکسی»(Chemotaxis) است که در آن سلولهای ایمنی، تومور را شناسایی میکنند و به سمت آن میروند تا حمله کنند. کموتاکسی توسط پروتئینهای کوچکی موسوم به «سیتوکینها»(Cytokines) هدایت میشود که به سایر سلولهای ایمنی سیگنال میدهند. «کموکینها»(Chemokines) زیرمجموعهای از سیتوکینها هستند که به انتقال سلولهای ایمنی کمک میکنند.
کموکین موسوم به «CXCL۱۶»، سلولهای T را که به گلبولهای سفید برای مبارزه با عفونت و سرطان کمک میکنند، برای نفوذ به سلولها به کار میگیرد. این موضوع نشان داده شده است که CXCL۱۶ و گیرنده آن موسوم به «CXCR۶»، میزان بقا را در بیماران مبتلا به سرطان روده بزرگ و ریه بهبود میبخشند. پژوهشهای اخیر نشان میدهند که CXCL۱۶ و CXCR۶ به همراه یکدیگر، ایمنی ضد تومور را ایجاد میکنند. با وجود این، هیچ کس روشی را برای انتقال CXCL۱۶ به محیط سلولی تومور کشف نکرده است.
دانشمندان مدتی است که میدانند برخی از گونههای باکتری میتوانند درون تومورها زنده بمانند. پژوهشگران دانشگاه کلمبیا از این دانش استفاده کرده و آن را با مهندسی ژنتیک ترکیب کردهاند تا باکتریها بتوانند سلولهای ایمنی بدن را برای هدف قرار دادن و از بین بردن تومورها به کار بگیرند.
دکتر «نیکلاس آرپایس»(Nicholas Arpais)، از پژوهشگران این پروژه گفت: ما طی دههها پژوهش برای درک چگونگی ایجاد شدن یک واکنش ایمنی، برای توسعه درمانهایی تلاش کردهایم که هر یک از آن مراحل مجزا را به طور ویژه هدف قرار میدهند.
موضوع مهم در این پژوهش، معرفی یک سویه پروبیوتیکی مهندسیشده از باکتری «اشریشیا کلی»(E. coli) بود که در روده انسان رایج است. اشریشیا کلی طوری مهندسی شد که حاوی یک مدار «کافت»(Lysis) هماهنگشده باشد. این راهی برای بهرهبرداری از توانایی ذاتی برخی باکتریها به منظور حمله به مکانهای بیماری در بدن است. کافت به تخریب یک یاخته در اثر از بین رفتن غشای بیرونی آن گفته میشود.
هنگامی که باکتریها به تومور وارد میشوند، مدار فعال میشود و به از هم پاشیدن یا کافت آنها میانجامد. کافت، تحویل موضعی مکرر کموکینها را امکانپذیر میسازد که سلولهای T را جذب میکنند و ایمنی ضد تومور را افزایش میدهند.
این گروه پژوهشی در سال ۲۰۱۹، یک سویه از باکتریهای غیر بیماریزا را مهندسی کردند تا مانند اسب تروا عمل کنند و به تومورهای موش وارد شوند تا از درون به آنها حمله کنند. آنها دریافتند که باکتریهای مهندسیشده، تومورها را پاکسازی میکنند و میزان متاستاز تومور را کاهش میدهند.
پژوهشگران در این پروژه علاوه بر به کار بردن یک باکتری مهندسیشده، بیان CXCL۱۶ را با یک کموکین دیگر به نام «CCL۲۰» ترکیب کردند. کموکین CCL۲۰، لنفوسیتها را جذب میکند. لنفوسیتها، سلولهایی قوی هستند که مسئولیت آغاز کردن واکنش ایمنی تطبیقی را با ارائه آنتیژن به سایر سلولهای ایمنی بر عهده دارند.
پژوهشگران دریافتند که ترکیب این دو کموکین، اثر درمانی آنها را افزایش میدهد و واکنش ایمنی نسبت به تومور را به گونهای تقویت میکند که پیشتر در دسترس نبوده است.
آرپایس گفت: با جفت شدن یک نوع سلول ایمنی ذاتی حیاتی با کموکینهایی که باعث نفوذ و فعالسازی سلولهای دندریتیک میشوند، امکان تشخیص دادن آنتیژنهای تومور افزایش مییابد.
آزمایشهای این گروه پژوهشی روی موشها نشان داد که باکتریهای مهندسیشده، یک واکنش ایمنی قوی را در برابر تومورهایی تولید میکنند که باکتریها مستقیما به آنها تزریق شدهاند و همچنین تومورهای دورتر که باکتریها به آنها تزریق نشدهاند. نکته مهم این است که باکتری بر بافت سالم تأثیر نمیگذارد.
آرپایس ادامه داد: آنچه میبینیم این است که باکتریها فقط محیط تومور را مستعمره خود میکنند و فقط به حد نصاب کافی برای ایجاد کافت در تومور میرسند. بنابراین، ما نمیتوانیم باکتریها را در اندامهای سالم تشخیص دهیم.
پژوهشگران در نظر دارند به تکمیل کردن روش خود با هدف استفاده از آن در آزمایشهای بالینی انسانی ادامه دهند.
این پژوهش، در مجله «Science Advances» به چاپ رسید.
منبع:ایسنا